
2020-04-26 17:04
昨日!商務部、海關、市場監督管理總局聯合公告(2020年第12號,4月26日起加強非醫用口罩出口質量監管,公告全文如下。
在全球疫情持續蔓延的特殊時期,為更有效支持國際社會共同應對全球公共衛生危機,現就進一步加強防疫物資質量監管、規范出口秩序有關措施公告如下:
一、加強非醫用口罩出口質量監管。自4月26日起,出口的非醫用口罩應當符合中國質量標準或國外質量標準。
商務部確認取得國外標準認證或注冊的非醫用口罩生產企業清單(中國醫藥保健品進出口商會網站www.cccmhpie.org.cn動態更新),市場監管總局提供國內市場查處的非醫用口罩質量不合格產品和企業清單(市場監管總局網站www.samr.gov.cn動態更新),非醫用口罩出口企業報關時須提交電子或書面的出口方和進口方共同聲明(參考附件1),確認產品符合中國質量標準或國外質量標準,進口方接受所購產品質量標準且不用于醫用用途,海關憑商務部提供的企業清單驗放,對不在市場監管總局提供的企業清單內的,海關接受申報,予以驗放。
對4月26日之前已簽訂的采購合同,出口報關時須提交電子或書面的出口方和進口方共同聲明(參考附件1)。
二、進一步規范醫療物資出口秩序。自4月26日起,產品取得國外標準認證或注冊的新型冠狀病毒檢測試劑、醫用口罩、醫用防護服、呼吸機、紅外體溫計的出口企業,報關時須提交書面聲明(參考附件2),承諾產品符合進口國(地區)質量標準和安全要求,海關憑商務部提供的取得國外標準認證或注冊的生產企業清單(中國醫藥保健品進出口商會網站www.cccmhpie.org.cn動態更新)驗放。
以上防疫物資出口質量監管措施將視疫情發展情況動態調整。
商務部 海關總署 國家市場監督管理總局
2020年4月25日
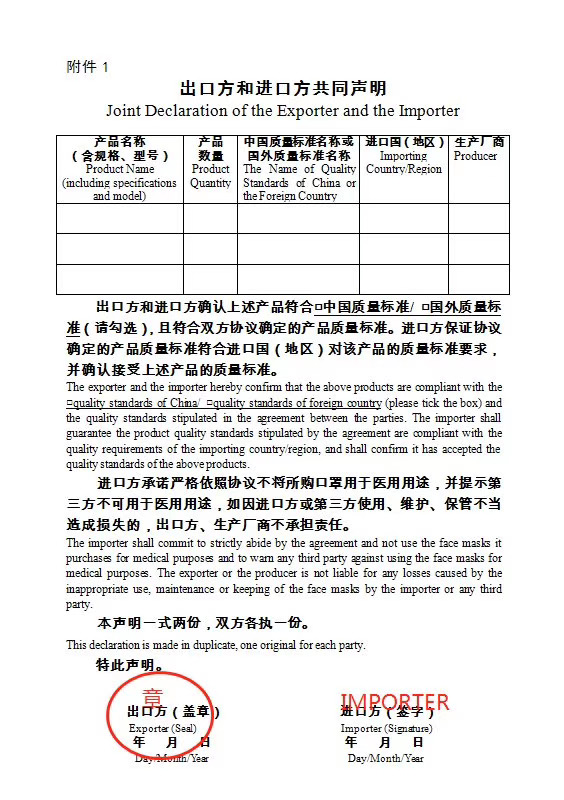
附件1:出口方和進口方共同聲明
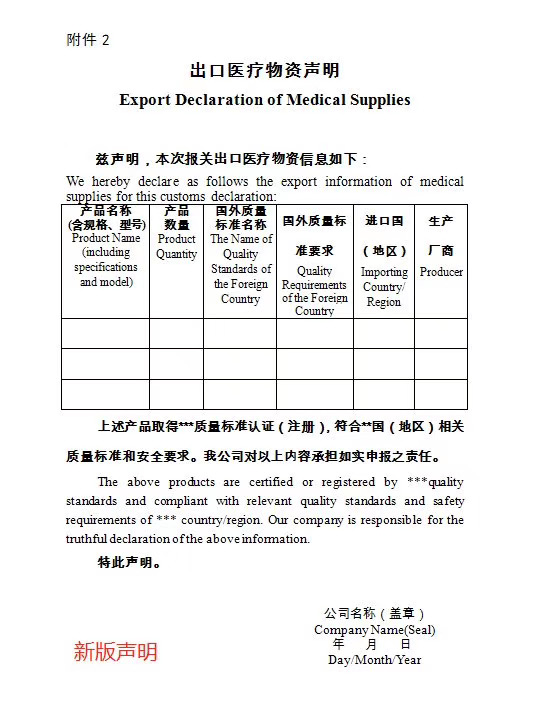
附件2:出口醫療物資聲明
對于新政策的推出,可以分兩部分進行解讀:
第一部分:非醫用口罩
25日晚24點前已經進監管區尚未放行的貨物。需要買賣雙方簽署《出口方和進口方共同聲明》,而后可被獲準放行而不受名單影響。但是如果在不合格名單范圍中,則可能還是不允許出口。
4月26日0點后申報出口的貨物,必須同時滿足以下三個條件:
1、在商務部確認取得國外標準認證或注冊的非醫用口罩生產企業清單范圍內或符合國內質量標準;
2、不在市場監管總局提供國內市場查處的非醫用口罩質量不合格產品和企業清單內;
3、需要買賣雙方簽署《出口方和進口方共同聲明》。
對于非醫用口罩應當符合中國質量標準或國外質量標準的要求,應該分為三種情況:1、國外強制要求執行相關標準的,并且采用生產商準入制度的,則應以公布名單為準。2、國外官方認可中國質量標準予以替代的,比如美國FDA的緊急使用授權法案就明確,符合YY/T0969的用于醫護領域的就不用FDA認證,歐盟也是符合GB2626的用于醫護的現在不用辦CE。3、國外對非醫用口罩無相關執行標準的,則必須符合中國質量標準。
所以,中國質量標準和境外標準不是“或”的關系。對于符合中國質量標準的判定,可能需要以第三方檢測機構的報告為宜,目前還未看到海關可以以企業自檢報告作為替代的,當然不排除執行差異問題。
第二部分:醫療器械
自4月26日0時起,出口包括醫用口罩在內的2020年第5號公告的醫療物資范圍中的產品,在公告基礎上增加了以下兩項要求:
1、商務部提供的取得國外標準認證或注冊的生產企業清單;
2、出口醫療物資聲明。
這意味著企業既要中國的醫療器械注冊,還要符合境外的標準認證或注冊,并納入國外官方準入清單。
嚴格要求境外注冊從公告中提到的《國外標準認證或注冊的非醫用口罩生產企業清單》來看,非醫用口罩也必須取得進口國官方的注冊和企業準入,這將進一步提高對非醫用口罩的監管要求,而這個要求則符合業內人士在之前的猜測,即對出口產品的監管責任主要在于進口國,只要進口國認可了產品或生產企業,中國海關沒必要再做限制性措施。
特別提醒
在公告中有一個特殊的措辭 “對4月26日之前已簽訂的采購合同” ,對于這個合同簽署節點確認的問題,海關應該是無法確定的,所以可能會以是否已經申報作為標志進行 “一刀切” 的判斷;也很可能海關以申報時間為準。當然,這只是一種猜測,具體還要以執行為準, 這個問題的執行就有待海關進一步明確了。
我們珍惜您每一次在線咨詢,用專業的知識,解答您的退稅難題。
讓您真正感受到我們的與眾不同!


